大分三愛メディカルセンター消化器病・内視鏡センターではセンター開設当初から膵癌の早期発見に積極的に取り組み、多くの患者さんに早期診断・治療を提供してきました。直近3年での当院医師による上皮内癌を含む10mm以下の早期膵癌の診断数は20例を超えており、全国レベルで見ても非常に高い診断能力を有しております。また、数々の学会発表・英語論文を通してその診断技術を発信しています.ここでは当センターで行われている、膵癌早期診断のプロセスをご紹介いたします。
大分三愛メディカルセンター三愛総合健診センター
- HOME
- 治療・手術内容について
- 早期膵癌発見に対する当院の取り組み
早期膵癌発見に対する当院の取り組み
目次
1. 全ての臓器癌の中で最も早期発見が大切な膵癌。早期膵癌とは?
そもそも膵癌とはどれくらい危険な病気でしょう。
- 国立がん研究センターの統計によると2018年の日本での膵癌新規罹患者数は42,000人を超えており、年々増え続けています。[ ≫詳しくはこちら ]
- 他の臓器の癌に関しては早期発見の技術や新規治療の開発などにより予後は改善されてきている一方で、膵癌の5年生存率は10%未満、つまり膵癌と診断された5年後には10人中1人生き残れるかどうかという状況であり、固形臓器癌の中で最悪の予後であると言われています[1-3]。
- 実際に膵癌は現在の日本の癌での死亡原因の第4位となっております。アメリカでも第3位となっており、数年後には更に順位が上がる予想となっています[2]。
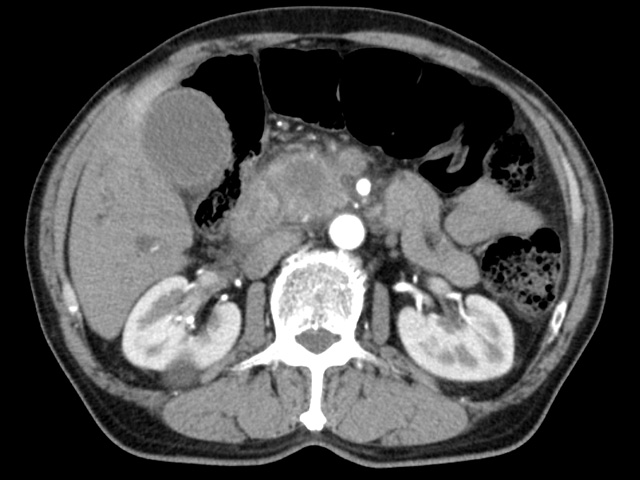
早期発見できた場合の予後はどのくらい?
- 膵癌の専門家の間では早期発見とは10mm以下の腫瘍で診断できたものを指します。
- ステージで言うとステージ0と1の一部のことを言います。
- それらが早期と呼ばれる理由は、10mm以下で治療できた場合の5年生存率は80%を超えると言われているからです[4, 5]。
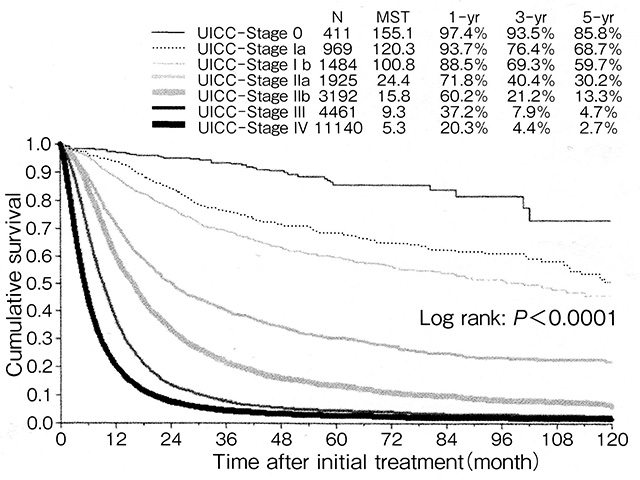
[4]より引用
- 膵癌全体の5年生存率が10%ないことを考えると10mm以下での発見がどれだけ重要か分かって頂けると思います。
- しかしながら膵癌全体における早期膵癌の割合は5%に満たず、発見が非常に困難とされています[4]。
- 様々な最新の技術を駆使して、何とか10mm以下の早期膵癌を見つけることが我々の喫緊の課題とされています。
2. 同じ膵癌でも違う?通常型膵癌とIPMN由来癌
膵癌のもとになる病変とは
- 膵癌には大きく分けて2種類の発生に関わる病変があります。
- PanIN:Pancreatic Intraepithelial neoplasia 膵管上皮性腫瘍
- IPMN:Intraductal Papillary Mucinous neoplasm 嚢胞性腫瘍
- これらは前癌病変(癌になる前の病変)と呼ばれており、ここから将来的に膵癌が発生する可能性が高いため厳重な経過観察が必要と言われています[6, 7]。
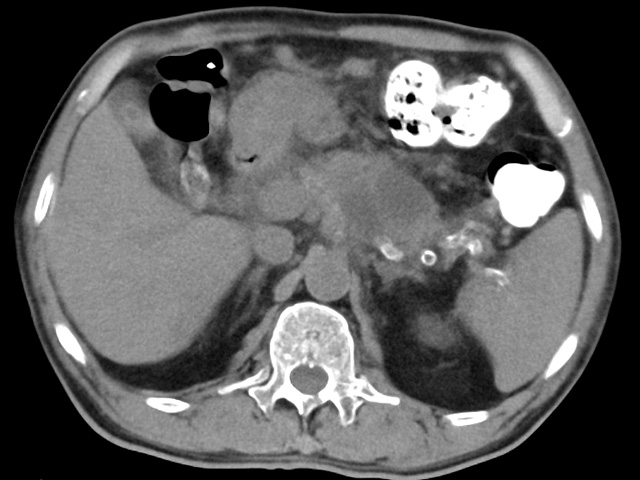
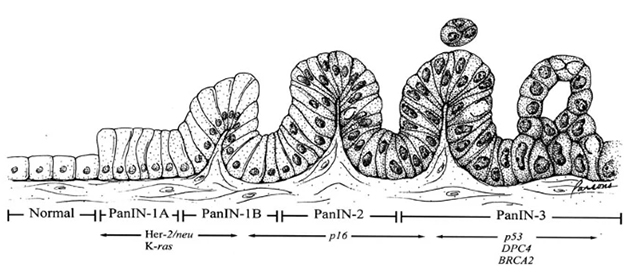
PanINとIPMNから発生する癌、どちらが見つかりやすい?
- PanINは進行すると高度異型を持つPanINつまり膵上皮内癌(ステージ0癌)となります。
- 膵上皮内癌は海外ではHigh-grade PanINやPanIN-3と呼ばれており、手術が必要な病変と言われています[7]。
- この状態では癌細胞は膵管上皮にのみ存在していますが、癌細胞が粘膜の下に浸潤すると浸潤癌(ステージ1-4の癌)へと進行します。
- PanINの膵癌への進展が一般的に通常型膵癌と呼ばれる腫瘍発育のルートです。
- IPMNも同様に進行すると高異型度のIPMNとなり、癌細胞が粘膜下に浸潤すると通常型膵癌と同様浸潤癌となります。こちらはIPMN由来癌と呼ばれ、IPMNという嚢胞性の腫瘍をもとに発育する癌です。
- どちらも同じ膵癌という括りではありますが、IPMNは悪性ではない初期病変でも明らかな嚢胞として様々な画像検査で見つけられる病変であり発見とその後の追跡が可能であるため、膵癌が出現した場合の発見も比較的容易です。
- 一方、膵上皮内癌は膵管の上皮内にのみ存在する癌であるため、腫瘤や明らかな嚢胞など分かりやすい発見の手がかりがありません。
- わずかな膵管の変化や周囲膵実質の変化のみから診断する必要があるため、IPMNに比べPanINの発見は非常に困難となります[8]。
3. 早期膵癌発見の手がかり。症状はある?リスク因子とは?
早期膵癌の症状
- 自覚症状は軽い腹痛、背中の痛み、体重減少、吐き気など膵癌に特徴的ではなく、例えば胃潰瘍などの消化管の病気でも現れる、ありふれたものです[5, 10]。
- 早期膵癌が原因で何らかの自覚症状が現れる患者さんは全体の25%程度と言われています。
- つまり残りの75%の方は自覚症状がないため、その他の徴候から診断する必要があります[5, 10]。ではどのようにして早期膵癌を発見すれば良いのでしょうか。
早期膵癌のリスク因子とは?
- 現在までに様々な研究が行われ、膵癌のリスク因子が同定されています。これらの因子をヒントに早期膵癌を見つけていくことの有用性も徐々に示されつつあります[5, 10, 11]。
- 家族歴や生活習慣に関わることとしては
などが挙げられます[11-13]。
膵癌の家族歴
多量飲酒(1日37.5g以上、ビール750ml以上)
喫煙
肥満
- 病歴に関わることリスクとしては
といった因子が挙げられます[11-13]。
糖尿病(特に新しく診断を受けた。急に数値が悪くなった)
慢性膵炎
IPMN
膵のう胞
遺伝性膵炎・膵癌症候群
- 特に前述のIPMNに関してはのう胞性そのものの癌化にも注意が必要ですが、IPMN以外の場所に通常型膵癌(PanIN由来癌)が発生するケースもあり、どちらの膵癌の発生にも注意が必要です[14]。
各リスク因子の膵癌発見に関わる危険度 膵癌家族歴 1.7-2.5倍 家族性膵癌(親兄弟に2人) 約7倍 糖尿病 約2倍 糖尿病発症から2年 5-8倍 糖尿病増悪 2倍 アルコール≧37.5g/day(ビール750ml) 1.2倍 喫煙 1.2-1.7倍 肥満 1.4-2.6倍 慢性膵炎 3-13倍 IPMN 約17倍 膵嚢胞 3-22倍 遺伝性膵炎/膵癌症候群 4-132倍 [11-13]より抜粋、改変。各リスク因子の膵癌発見に関わる危険度
- 血液検査で分かるものとしては膵酵素(アミラーゼ・エラスターゼ)の上昇や腫瘍マーカー(CEA/CA19-9)の上昇などがあります[10, 12, 15]。
- これらのリスク因子は日常的に気を配ることが出来るものから、健診などを含め医療機関を受診しなければ分からないものまで様々です。
- 当院では上記のような様々な因子を多角的に評価し、患者さんに対し早期膵癌を発見するための検査を推奨しており、リスク因子と症状を組み合わせたスコアリングシステム[11]を使いながら、膵癌リスクが高いと判断した患者さんに対して膵臓の画像検査をお勧めしています。
- このスコアリングシステムに関する検討は、当院を中心として現在全国10施設の病院で多施設共同研究が行われています。
4. 画像検査から早期膵癌を発見する。どんな画像検査が必要?
健診などで行われる画像検査
- 最も一般的な検査は腹部超音波検査です。おなかに超音波プローブを当て、膵臓を観察します。
- 少量の被爆で多くの情報が得られるものとして単純CT検査があります。
- しかしながらこれらの検査では20-30mm程度ある程度の大きさの膵癌を発見することは出来ますが、早期膵癌の発見はほぼ不可能です。
- 膵管拡張や嚢胞といった膵癌に伴う間接所見をある程度指摘することは可能です。
早期膵癌診断に必要な3つのキー画像検査
腹部造影CT検査
血管と膵組織、腫瘍とのコントラストをつけて診断するために血管の中に造影剤という薬剤を注入して検査する方法です。
- 通常型膵癌は線維化の強い腫瘍であるため、血流が少なく造影剤が腫瘍内にあまり流入せず、造影不良域として認識されるため診断ができます。
- 膵実質の萎縮を捉えることができます。
- 放射線被ばくを考慮する必要があります。
MRI(MRCP)検査
腫瘍本体よりも膵管拡張や嚢胞といった膵癌に付随する間接所見を詳細に指摘することが可能です。実際、膵癌の半数以上の症例は膵管拡張を伴っています[8]。
- 画像を再構成することで、主膵管を連続的に描出でき、嚢胞などとの位置関係を捉えられるのが大きな強みです。
- 腫瘍自体を描出することもできますが、早期膵癌自体を描出する能力は高くありません。
- 放射線被ばくがありません。
超音波内視鏡検査(EUS)
現存する画像検査の中で微小腫瘍、膵管変化、嚢胞などを最も高い確率で指摘できるものです。10mm以下の微小腫瘍も比較的はっきりと描出することが可能です。
- 造影剤などを用い、リアルタイムで腫瘍の評価が可能です。
- 検査を行う内視鏡医の力量に検査の質が左右される可能性があります。
- 胃カメラよりもやや太い内視鏡を用いるため、やや侵襲的です。
- 各々の検査で良い点・悪い点がありますが、特に早期膵癌診断に関しては全ての検査を行い、多角的に病変を捉える必要があります。
5. 画像検査で見逃してはならない早期膵癌の特徴
小さい腫瘍は画像検査で描出できるか?
- 早期膵癌は10mm以下の浸潤癌ないしは腫瘤を形成しない上皮内癌を指します。
- 造影CT、MRI、EUS検査を用いても腫瘍自体を捉えきれないことが多くあります。特に上皮内癌は腫瘍を形成しないものであるため、描出はほぼ不可能です。
- 早期膵癌診断、特に上皮内癌の診断には間接所見つまり、癌が原因で起こってくる膵臓の変化を細かく診断する必要があります。
膵管狭窄・膵管拡張
- 上皮内癌が膵管内に形成されると膵管内を流れる膵液(消化液)の流れが滞ります。
- 流れが悪くなることで病変周囲の細かい膵管内には症状を感じないような小さい炎症が繰り返されることが予想されています。
- 膵管周囲に炎症が起こるとその周囲に線維化が起こります。また、炎症の影響で主膵管が細くなります(膵管狭窄)
- さらに狭窄より尾側(膵液の流れの上流)の膵管は流れが悪くなることで拡張します。
- 膵管狭窄・尾側膵管の拡張は造影CT、MRI、EUSで捉えることができ、早期膵癌、特に上皮内癌診断に重要な所見です[5, 8, 15, 16]
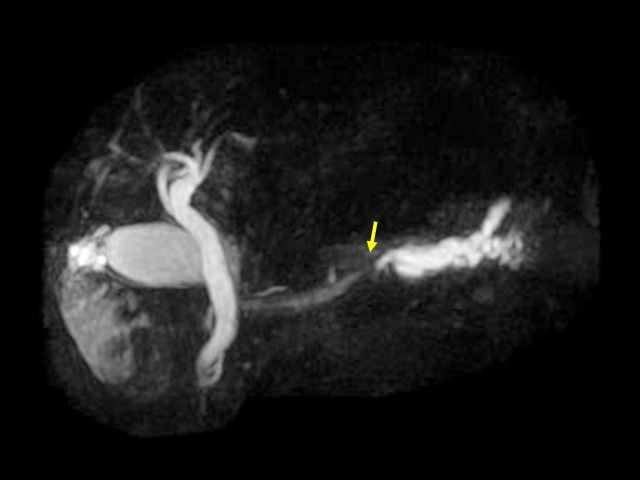
上皮内癌のMRI検査にMRI検査における、主膵管の狭窄(黄色矢印)と尾側の著名な膵管拡張
限局性膵実質萎縮
- 膵管狭窄の項でも述べた通り、上皮内癌が存在する膵管周囲の炎症はまわりの膵実質まで波及し、線維化を引き起こす上に、膵実質部分の正常細胞は崩れてしまいます。
- 病変周囲の膵実質がくびれるように萎縮する(痩せてくる)所見は早期膵癌診断の重要な所見です[8, 16-18]。
- 造影CTで最もうまく捉えることができます。
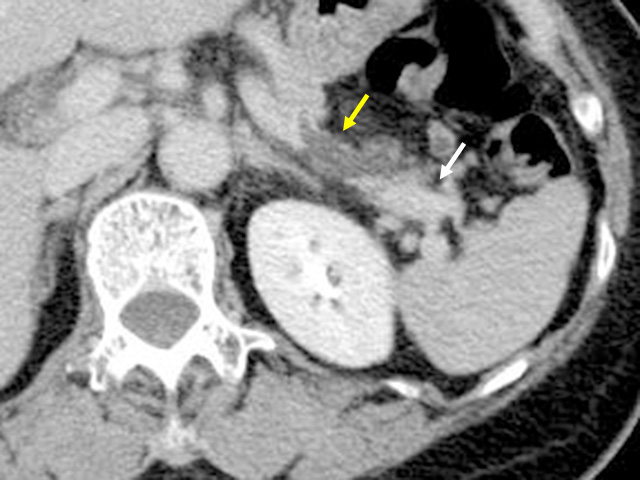
上皮内癌では、造影CTで、拡張した膵管周囲の膵実質は萎縮して削げ落ちています(黄色矢印)。
さらに尾側の膵実質はある程度確認できます(白色矢印)。
貯留嚢胞(分枝膵管拡張)
- 上皮内癌が膵管内に形成されることで膵液の流れが滞ることは前項でも説明しましたが、それにより分枝膵管(膵管の枝)に膵液が溜まることもあります。
- 上皮内癌周囲には貯留嚢胞と呼ばれる小さな分枝膵管の拡張がばらばらと認められることが多く、これも早期膵癌発見のための重要な因子です[5, 8, 15, 16]。
- MRI、EUSで最もうまく捉えることができます。
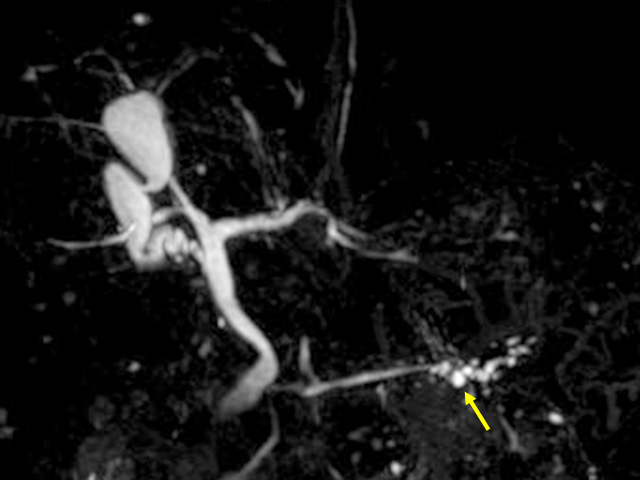
MRIで膵管狭窄周囲に出現した貯留嚢胞(黄色矢印)
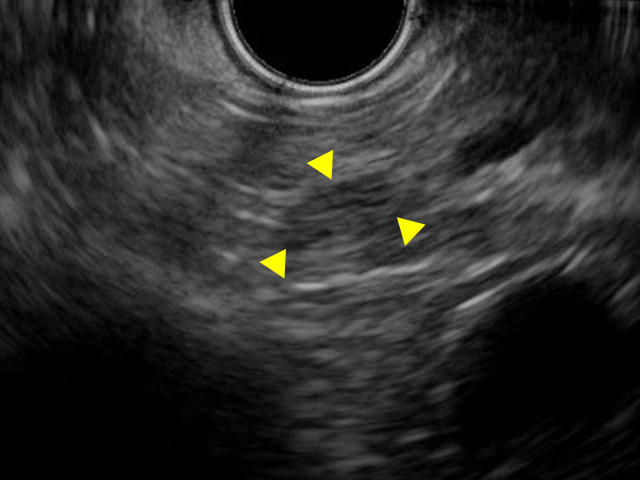
膵管周囲低エコー
- EUSでのみ見られる所見で、上皮内癌周囲の膵実質の細胞脱落や線維化の程度が強まるとみられる所見と言われています。
- 術者により差があるものの、明らかな所見を持つ上皮内癌の診断には有用です[8, 16, 19]。
膵管狭窄・拡張
- 限局性膵実質萎縮・貯留嚢胞(分枝膵管拡張)、膵管周囲低エコーの所見が複数指摘出来た場合は、早期膵癌発見の可能性が非常に高くなるため[8, 16]、最終的な術前診断である、細胞診検査を行います。
6. 早期膵癌における最終診断を担う細胞診検査とは?
- これまで述べてきた画像所見では早期膵癌が存在する可能性が高いことまでは分かりますが、画像的に強く疑われる=手術ということにはなりません。
- 膵切除の手術は非常に侵襲的(体への負担が大きいため)であるため、手術をして癌はありませんでしたということを限りなく0に近づける必要があります。
- 病理細胞学的な検査を行うことで、画像所見に加え、より正確に早期膵癌の術前診断を行うことができます。
超音波内視鏡下穿刺吸引細胞診・生検(EUS-FNAB)
- EUSで腫瘍が認識できる場合、つまり微小浸潤癌の場合は針で細胞と組織を採取する方法が有用であり、殆どの施設でまずこの検査が行われます。
- 針で腫瘍を突き刺して得た細胞と組織をそれぞれ病理学的に判定し、膵癌または膵癌の疑いが強いという診断結果の場合は早期膵癌の可能性が飛躍的に高まります。
- しかしながら10mm以下の浸潤癌に対するこの検査の感度は40-70%程度との報告もあり、EUS-FNABで診断のつかない症例もあります[15]。
- 非常に低い確率ではありますが、消化管穿孔・出血・膵炎及び穿刺した針から癌細胞が消化管内に植えつけられる(needle tract seeding)などの合併症が起こるリスクがあります。
- 上皮内癌を含む早期膵癌診断に有用とされているのが膵液細胞診検査です。
膵液細胞診検査
- 逆行性胆管膵管造影検査(ERCP)と呼ばれる検査をまず行います。
- この検査は内視鏡を十二指腸乳頭部(膵管の出口、膵液が流れ出る部分)まで挿入し、そこから造影剤を膵液の流れと逆向きに注入することで、膵管を直接描出します。
- 膵管内の膵液、更には膵管内にチューブを留置し、片方の鼻の孔から出すことで膵管と外を繋ぐことができます。
- 膵管内に流れる膵液を1晩かけて合計6回採取し、悪性細胞があるかどうかのの検査を行います。前項同様、膵癌または膵癌の疑いが強いという診断結果の場合は早期膵癌の可能性が飛躍的に高まります。
- しかしながら癌が存在する部位までは分からないという難点があります。
- 非常に低い確率ではありますが、消化管穿孔・出血・などの合併症が起こるリスクがあります。
- 比較的高い確率(7%程度)で軽症の膵炎合併症が起こるリスクがあります。重症化することは極めて稀です[15]。
7. 早期膵癌の治療法は?
- 早期膵癌の治療は現時点では膵切除のみです。
- 画像的に早期膵癌が最も疑わしいところを病変と予想して切除を行うため、場所により膵頭部からの切除になるか、尾部からの切除になるかが変わります。
- 膵体尾部切除術は比較的低侵襲ですが、膵頭十二指腸切除術は膵頭部を切除するとともに十二指腸・胆管を切除し、それらを別の消化管に繋ぎなおす大掛かりな手術になります。
- いずれも腹腔鏡による治療が検討できます。
- 当院は東京女子医科大学附属病院 肝胆膵外科 教授の本田五郎先生と医療連携を行っており、患者さんには日本トップレベルの外科手術を受けて頂くことができます。(≫本田五郎先生HP )

切除病変の分枝膵管の病理所見の一部。丈の高い乳頭状の細胞が核配列の乱れと共に増生しており、High-grade PanIN:上皮内癌の診断となった。
8. 早期膵癌治療の限界
- 精細な画像診断、病理細胞学的診断をもってしても早期膵癌の100%の診断は出来ません。
- 非常に少数ではありますが、早期膵癌を強く疑い手術を行ったが、取った膵臓に癌細胞がないということもあります。
- もちろんそのような状況でもPanINは存在しているため、それらが将来的に癌化するリスクは防げます。
- また切除した膵臓を細かく切って病理検査を行うのにも限界があります。切れていない部分に癌細胞が存在する可能性も大いにあります。
- 患者さんにはあらゆる可能性をお話しした上で、ご希望の場合のみ手術治療を受けて頂いております。
9. 早期膵癌診断を発信する。国内・国際学会・論文発表
- 早期膵癌診断・治療の分野は日本のきめ細かな診療が成せる技であり、日本から世界への発信が必要な分野です。
- 当院でも国内・国際学会や論文発表を通して、国内外を問わず、少しでも多くの消化器内科の医師に知識共有をさせて頂く取り組みを行っております。
- 若手胆膵専門医師による早期膵癌に対する診断、治療を研究するグループとして2020.4に結成されたPASSYON(Pancreatic Cancer Research for Secure Salvage Young Investigators)において当院の医師である佐上亮太はコアメンバーを務め、若手医師の早期膵癌関連の知識共有・啓発・論文作成などを積極的に行っている
論文
- Pre-Operative Imaging and Pathological Diagnosis of Localized High-Grade Pancreatic Intra-Epithelial Neoplasia without Invasive Carcinoma.
Sagami R, Yamao K, Nakahodo J, Minami R, Tsurusaki M, Murakami K, Amano Y. Cancers (Basel). 2021; 13: 945. - Utility of Endoscopic Ultrasonography Screening for Small Pancreatic Cancer and Proposal for a New Scoring System for Screening.
Sagami R, Nishikiori H, Anami K, Fujiwara S, Honda K, Ikuyama S, Kitano M, Murakami K. Pancreas. 2018; 47:257-264.
学会発表
- 2021.11 Japan Digestive Disease Week (JDDW)
膵癌早期診断のためのスコアリングシステムの運用
発表形式:シンポジウム - 2021.9 第52回 日本膵臓学会大会
膵癌早期診断のためのスコアリングシステムの運用
発表形式:シンポジウム - 2021.5 第101回 日本消化器内視鏡学会総会
膵上皮内癌における超音波内視鏡所見の検討-間接所見を描出する-
発表形式:ワークショップ - 2021.1 第51回日本膵臓学会大会
リスク複合を考慮した膵癌診断スコアリングシステムの前向き研究~Stage0癌の診断率~
PanCan Clinical Investigator Award受賞 - 2020.12 日本消化器内視鏡・消化器病学会 九州支部例会
各種画像診断における上皮内癌(Stage0)の特徴-EUS・CT・MRI・ERPを使いこなす-
発表形式:ワークショップ - 2019.7 第50回日本膵臓学会大会
膵癌スクリーニングのための新規スコアリングシステムの検証
発表形式:ミニシンポジウム - 2017.7 日本膵臓学会 Young Investigator Award受賞
膵癌早期診断におけるEUSの有用性とスクリーニングのための新スコアリングシステムの提案発表形式:Awardセッション - 2017.5 日本内視鏡学会 総会
当院におけるT1膵悪性腫瘍の診断ストラテジー 発表形式:口演 - 2017.4 第103回日本消化器病学会 総会
生活習慣病を考慮した早期膵癌スクリーニングのためのスコアリングシステムの提案
発表形式:口演
10.参考文献
- Siegel RL, Miller KD, Fuchs HE et al. Cancer Statistics, 2021. CA Cancer J Clin 2021; 71: 7-33. doi:10.3322/caac.21654
- Rahib L, Smith BD, Aizenberg R et al. Projecting cancer incidence and deaths to 2030: the unexpected burden of thyroid, liver, and pancreas cancers in the United States. Cancer Res 2014; 74: 2913-2921. doi:10.1158/0008-5472.Can-14-0155
- Xiao AY, Tan ML, Wu LM et al. Global incidence and mortality of pancreatic diseases: a systematic review, meta-analysis, and meta-regression of population-based cohort studies. Lancet Gastroenterol Hepatol 2016; 1: 45-55. doi:10.1016/s2468-1253(16)30004-8
- Egawa S, Toma H, Ohigashi H et al. Japan Pancreatic Cancer Registry; 30th year anniversary: Japan Pancreas Society. Pancreas 2012; 41: 985-992. doi:10.1097/MPA.0b013e318258055c
- Kanno A, Masamune A, Hanada K et al. Multicenter study of early pancreatic cancer in Japan. Pancreatology 2018; 18: 61-67. doi:10.1016/j.pan.2017.11.007
- Basturk O, Hong SM, Wood LD et al. A Revised Classification System and Recommendations From the Baltimore Consensus Meeting for Neoplastic Precursor Lesions in the Pancreas. Am J Surg Pathol 2015; 39: 1730-1741. doi:10.1097/pas.0000000000000533
- Ren B, Liu X, Suriawinata AA. Pancreatic Ductal Adenocarcinoma and Its Precursor Lesions. The American Journal of Pathology 2019; 189: 9-21. doi:10.1016/j.ajpath.2018.10.004
- Sagami R, Yamao K, Nakahodo J et al. Pre-Operative Imaging and Pathological Diagnosis of Localized High-Grade Pancreatic Intra-Epithelial Neoplasia without Invasive Carcinoma. Cancers (Basel) 2021; 13. doi:10.3390/cancers13050945
- Klein WM, Hruban RH, Klein-Szanto AJ et al. Direct correlation between proliferative activity and dysplasia in pancreatic intraepithelial neoplasia (PanIN): additional evidence for a recently proposed model of progression. Mod Pathol 2002; 15: 441-447. doi:10.1038/modpathol.3880544
- Ikemoto J, Serikawa M, Hanada K et al. Clinical Analysis of Early-Stage Pancreatic Cancer and Proposal for a New Diagnostic Algorithm: A Multicenter Observational Study. Diagnostics (Basel) 2021; 11. doi:10.3390/diagnostics11020287
- Sagami R, Nishikiori H, Anami K et al. Utility of Endoscopic Ultrasonography Screening for Small Pancreatic Cancer and Proposal for a New Scoring System for Screening. Pancreas 2018; 47: 257-264. doi:10.1097/mpa.0000000000000988
- Yamaguchi K, Okusaka T, Shimizu K et al. Clinical Practice Guidelines for Pancreatic Cancer 2016 From the Japan Pancreas Society. Pancreas 2017; 46: 595-604. doi:10.1097/mpa.0000000000000816
- Matsubayashi H, Ishiwatari H, Sasaki K et al. Detecting Early Pancreatic Cancer: Current Problems and Future Prospects. Gut Liver 2020; 14: 30-36. doi:10.5009/gnl18491
- Kamata K, Kitano M, Kudo M et al. Value of EUS in early detection of pancreatic ductal adenocarcinomas in patients with intraductal papillary mucinous neoplasms. Endoscopy 2014; 46: 22-29. doi:10.1055/s-0033-1353603
- Hanada K, Okazaki A, Hirano N et al. Diagnostic strategies for early pancreatic cancer. J Gastroenterol 2015; 50: 147-154. doi:10.1007/s00535-014-1026-z
- Nakahodo J,Kikuyama M,Nojiri S et al. Focal parenchymal atrophy of pancreas: An important sign of underlying high-grade pancreatic intraepithelial neoplasia without invasive carcinoma,i.e.,carcinoma in situ. Pancreatology 2020; 20: 1689-1697. doi:10.1016/j.pan.2020.09.020
- Yamao K,Takenaka M,Ishikawa R et al. Partial Pancreatic Parenchymal Atrophy Is a New Specific Finding to Diagnose Small Pancreatic Cancer (≤10 mm) Including Carcinoma in Situ: Comparison with Localized Benign Main Pancreatic Duct Stenosis Patients. Diagnostics (Basel) 2020; 10. doi:10.3390/diagnostics10070445
- Kanno A,Masamune A,Hanada K et al. Advances in Early Detection of Pancreatic Cancer. Diagnostics (Basel) 2019; 9. doi:10.3390/diagnostics9010018
- Izumi Y,Hanada K,Okazaki A et al. Endoscopic ultrasound findings and pathological features of pancreatic carcinoma in situ. Endosc Int Open 2019; 7: E585-e593. doi:10.1055/a-0839-4312